中国科学院过程工程研究所生化工程国家重点实验室马光辉研究员、夏宇飞副研究员在总结课题组前期工作的基础上,提出肿瘤合成疫苗就像制造高端产品一样,在构建过程中要连接机体内固有的免疫供应链。相关思路总结为综述文章,应邀以“基于合成颗粒的癌症疫苗:联通免疫供应链(Synthetic particles for cancer vaccines: Connecting the inherent supply chain)”为题,在9月18日在线发表于Accounts of Chemical Research刊物上,并被遴选为封面文章,论文链接: https://dx.doi.org/10.1021/acs.accounts.0c00336。
疫苗合成学是生化室马光辉团队提出的疫苗构建新思路和新策略。团队认为对于肿瘤治疗性疫苗而言,如何利用合成颗粒联通机体抗肿瘤免疫应答的供应链是癌症疫苗研究的关键问题,即捕获癌细胞释放出肿瘤来源的抗原作为原料,加工并呈递到抗原递呈细胞(APC)中,传递给T细胞,激活T细胞转变为效应性的细胞杀伤性T细胞,并引起其在肿瘤部位的累积,杀伤肿瘤细胞。此时,癌细胞释放的额外的抗原重新作为合成颗粒设计的原料,从而联通了闭环的供应链。
然而,在癌症疫苗应用中,由于肿瘤抗原库失效、细胞毒性T细胞(CTL)反应受限、肿瘤内免疫抑制环境等多种因素的影响,会导致机体固有的供应链被阻断,从而影响肿瘤的治疗效果。为了解决这个问题,合理设计的颗粒疫苗,可以为体内免疫过程提供完整的物流系统,进而有望重新连接固有免疫供应链(图1):1)抗原的采购:强化肿瘤抗原的递送,将抗原转移至APC,依靠有效的APC内吞作用引流至淋巴结,为免疫细胞产生抗肿瘤作用提供原材料(肿瘤相关抗原);即设计合成颗粒不同的物化性质,例如正电荷、磁性靶向基团以及短棒状结构(图2a,b),局部产生炎症引发细胞募集,促进APC内吞作用从而引流至淋巴结。此外,通过设计小粒径颗粒(< 100 nm)也可以直接富集至淋巴结。原材料的有效摄取是为了之后的高效加工过程做准备,促进更好的活化和抗原递呈。2)制造:抗原通过APC识别和递呈,产生CTL。刺激APC的激活和抗原的交叉呈递以增强抗肿瘤细胞免疫反应,从而产生有效的CTL消除肿瘤细胞;在合成颗粒设计中引入柔性的仿生观念,如设计具有柔性的二维材料石墨烯以及同时具备柔性以及抗原流动性的颗粒稳定的Pickering乳液,促进APC细胞的识别,动态激活免疫响应(图2c,d)。此外在合成颗粒设计中,利用PLGA在酸性下的电荷反转或正电荷颗粒的质子化,引发大量H+内流,涨破溶酶体;或者利用特殊材料性质,如CaCO3产生内部气压,涨破溶酶体,从而引发溶酶体逃逸,促进抗原的交叉递呈(图2e,f)。原材料高效加工的最终目的是为了产品效应最优化,即产生多而强的肿瘤杀伤性T细胞。3)“营销”策略:通过加强CTL瘤内积累并逆转肿瘤内的免疫抑制微环境,最大程度地消除肿瘤细胞。在合成颗粒表面包被肿瘤细胞膜(图2g-i),或者通过磁靶向使CTL定向富集至肿瘤部位;或者联合递送免疫检查点抑制剂(PD-1等)诱导冷肿瘤向热肿瘤转化,从而逆转免疫抑制微环境,提高肿瘤杀伤效应,进而进一步强化抗癌效果。因此,该综述基于合成颗粒剂型的基础,系统研究了多种成分(抗原, 佐剂和 PD-1)的协同递送,以优化肿瘤免疫应答效果。
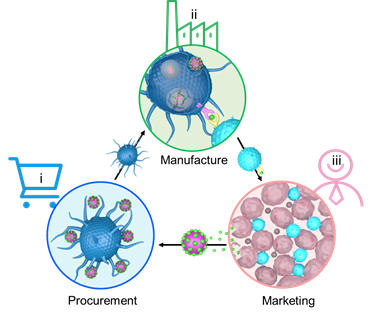
图1. 通过合成颗粒连接抗癌供应链的示意图:(i)采购:合成颗粒递送抗原至APC或者引流淋巴结从而激活APC。(ii)制造:合成颗粒可促进抗原交叉递呈,从而激活T细胞以发挥抗肿瘤作用。 (iii)销售:合成颗粒传递信号以促进在肿瘤内积累的足够的免疫细胞并刺激效应性T细胞增值,并逆转肿瘤微环境,增强抗肿瘤功效。
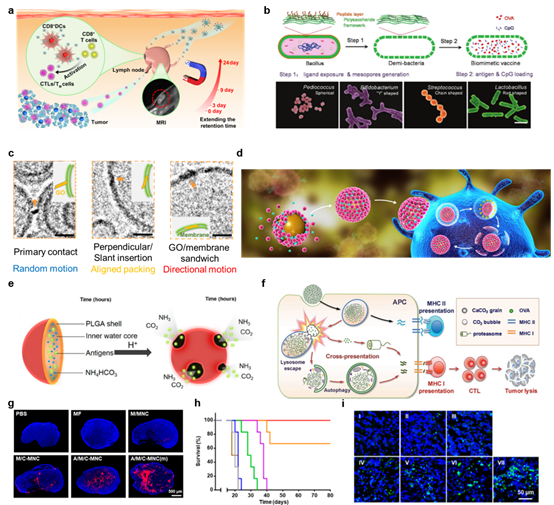
图2.(a)带有抗CD205修饰的癌细胞膜涂层磁性纳米簇(A / M / C-MNC)的示意图,磁靶向增强淋巴结停留时间;(b)制备不同形状的DB的水热过程示意图,短棒状颗粒能有效促进细胞内吞;(c)GO与APC膜的Cyro-TEM图像,表明柔性材料促进与膜的相互作用;(d)颗粒稳定的Pickering乳液同时具备柔性 与流动性,动态激活免疫响应;(e)PLGA在酸性下的电荷反转或者正电荷颗粒的质子化,引发大量H+内流,涨破溶酶体示意图;(f)CaCO3纳米颗粒的产气策略促进抗原交叉呈递示意图;(g)淋巴结的免疫组织化学分析,磁靶向增强抗原在淋巴结中的停留时间;肿瘤细胞膜包被的颗粒可增加T细胞表位的丰度并促进肿瘤杀伤作用,(h)生存曲线,表明有效的肿瘤抑制作用;(i)在4T1原发性肿瘤中肿瘤内CTL浸润的免疫组织化学分析,表明CTL充分浸润。
本综述的第一作者是夏宇飞副研究员和硕士研究生宋畑畑,通讯作者是马光辉研究员。基于生化室开发的合成颗粒技术,经过多年的系统研究,发现了合成颗粒的癌症疫苗设计的环形供应链策略,并构建了一系列疫苗新剂型。相关工作相继发表于Nature Materials(2018, 17, 187)、Advanced Materials(2018, 30, 1801067, Cover; 2019, 31, 1801159, Cover; 2020, 32, 2004210, Cover)、ACS Nano (2019, 13, 13809, Cover)等期刊上,部分工作正在积极地展开临床前研究。
附件下载: